Les QCM interactifs sont accessibles à partir de la page d’accueil
du coaching virtuel à accès gratuit dilingco.com
Page 1.
2 méthodes d’équilibrage
redox
Sélectionner
l’affirmation exacte :
1-
Calculer le nombre d’oxydation est indispensable pour équilibrer une réaction
d’oxydoréduction
2- Le
nombre d’oxydation (n.o.) est la charge électrique réelle ou fictive d’un
élément chimique
3- Le
nombre d’oxydation d’un ion est nul
4- Le
nombre d’oxydation d’une molécule est différent de 0
L’affirmation
2 est exacte.
Affirmation
1
Non.
2 méthodes sont à disposition pour équilibrer une
réaction d’oxydoréduction.
Les 2
méthodes donnent le même résultat.
Utiliser
le n.o. pour équilibrer une réaction d’oxydoréduction n’est donc pas
indispensable.
Mais,
dans une équation chimique, une variation du
nombre d’oxydation indique à coup sûr qu’il s’agit d’une réaction d’oxydation.
Le n.o.
permet aussi de déterminer l’élément qui s’oxyde.
(Élément qui s’oxyde = réducteur)
Affirmation
2
Oui.
Le nombre d’oxydation (n.o.) :
- aussi
appelé « degré d’oxydation », d.o.
- se note
conventionnellement en chiffres romains,
- est la charge électrique réelle ou fictive d’un élément
chimique,
- peut
apparaître dans les annotations:
Oxyde de
fer (II) : FeO, le fer a un n.o. = II
Oxyde de
fer (III) : Fe2O3, le fer a un n.o. = III
Ces
exemples montrent qu’un même atome peut avoir plusieurs valeurs de n.o. selon
la molécule où il se trouve.
Affirmation
3
Non.
Le nombre d’oxydation d’un ion est égal à sa charge électrique.
Exemples :
Cr3+,
n.o. = III
CIO4-,
n.o. = I
Affirmation
4
Non.
Une
molécule n’a pas de charge électrique : Le
nombre d’oxydation d’une molécule est nul.
Équilibrer
une demi-équation redox c’est :
- Equilibrer le nombre d’éléments
chimiques,
- Equilibrer le nombre de charges électriques,
- Si l’oxydant contient des atomes d’oxygène :
-
Placer des ions H+ coté oxydant,
-
Placer des molécules d’eau coté réducteur.
2
méthodes
Deux
méthodes d’équilibrage :
- Méthode
des nombres d’oxydation
(À
utiliser pour les couples redox d’éléments chimiques simples)
- Méthode
d’équilibrage direct par les 2 demi équations
Dans les deux procédures, commencer par équilibrer les éléments
chimiques.
Placement des électrons
Les deux
procédures divergent sur le moment où placer les électrons pour équilibrer les
charges électriques.
n.o :
placer les électrons au début, en fonction des
nombres d’oxydation,
½
équations : placer les électrons en fin de
procédure lorsque tous les composants sont placés et équilibrés.
Page 2.
Méthode équilibrage matières
Sélectionner
l’affirmation exacte :
1. [A]. Dans
un couple redox, l’oxydant est le composé chimique qui a le moins de charges
2. [B].
Conservation des éléments chimiques : commencer toujours par équilibrer
les éléments autres que O et H
3. [C].
Rajouter 5 électrons pour équilibrer les charges électriques
4. [D].
Rajouter O2 pour équilibrer les oxygènes
L’affirmation
2 est exacte.
Affirmation
1
Non.
[A]. L’oxydant :
- est celui qui est écrit à gauche du « / » (c’est une convention)
- est
celui qui dans la demi équation « obtient » les électrons pour se
réduire en réducteur
Rappels :
- un
oxydant …se réduit,
- se
réduit par une réaction de réduction pour former un réducteur.
Oxydation = perte d’électrons et formation d’un
oxydant.
Réduction = gain d’électrons et formation d’un réducteur.
Affirmation
3
Non.
[C].
Rajouter 6 électrons pour équilibrer les charges électriques.
Côté
gauche : 2 charges- + 14 charges+ = 12 charges+
Côté
droit : 6 charges+
Rajouter
6 e- côté droit pour équilibrer les charges.
Affirmation
4
Non.
[D]. Rajouter
2H2O pour équilibrer les oxygènes.
Pour
équilibrer l’excédent d’hydrogène causé par le rajout d’H2O, il
faut :
- rajouter de H en milieu acide,
-
rajouter des HO en milieu basique.
Équilibrer
une demi-équation redox c’est :
- Equilibrer le nombre d’éléments
chimiques,
- Equilibrer le nombre de charges électriques,
- Si l’oxydant contient des atomes d’oxygène :
-
Placer des ions H+ coté oxydant,
-
Placer des molécules d’eau coté réducteur.
2
méthodes
Deux
méthodes d’équilibrage :
- Méthode
des nombres d’oxydation
(À
utiliser pour les couples redox d’éléments chimiques simples)
- Méthode
d’équilibrage direct par les 2 demi équations
Dans les deux procédures, commencer par équilibrer les éléments
chimiques.
Placement des électrons
Les deux
procédures divergent sur le moment où placer les électrons pour équilibrer les
charges électriques.
n.o :
placer les électrons au début, en fonction des
nombres d’oxydation,
½
équations : placer les électrons en fin de
procédure lorsque tous les composants sont placés et équilibrés.
Page 3.
½ réaction. Méthode des
n.o.

Sélectionner
l’affirmation exacte :
1- Les
nombres d’oxydation sont à calculer pour tous les composants des éléments de la
½ équation
2- [A].
La différence de n.o. a été calculée pour 1 atome Cr, comme il y en a 2 côté
réactifs, il faut rajouter 2x(n.o) électrons
3- [B].
Différence de charges = 2
4- [C].
La ½ réaction est équilibrée du point de vue des charges et des matières
L’affirmation
2 est exacte.
Affirmation
1
Non.
Les nombres
d’oxydation sont à calculer pour l’élément,
présent des côtés oxydant/réducteur, caractéristique du couple
considéré ; ici Cr.
Il faut
bien entendu se rappeler les valeurs fondamentales des n.o. d’une molécule,
d’un ion, de l’atome d’oxygène et d’hydrogène.
Revoir chapitre Nombres d’oxydation
Affirmation
3
Non.
[B].
Différence de charges : 6+ - (-8) = 14 charges positives à rajouter côté
réactifs.
14 H+
sont rajoutés.
Affirmation
4
Non.
[C]. La ½
réaction sera équilibrée du point de vue des matières si on rajoute 2 H2O
côté produits.
Valeurs
n.o. à connaître
n.o. molécule = 0
n.o. ion = charge de l’ion
Le n.o. de l’atome d’oxygène est égal à –II
Exceptions :
-
les peroxydes (H2O2,
Na2O2, K2O2, …), n.o. = -I.
- le
dioxygène O2, n.o. = 0
Le n.o. de l’atome d’hydrogène est égal à +I.
n.o =+I car les atomes d’hydrogène, moins
électronégatifs, cèdent leur e- aux atomes liés d’électronégativité plus
élevée.
Exceptions :
- les hydrures, H combiné à un métal (NaH, LiH, KH,
…), n.o. = -I
- le
dihydrogène H2, n.o. = 0
Le n.o.
du fluor est toujours égal à –I.
Page 4.
Milieu acide. Milieu
basique
Sélectionner
l’affirmation exacte :
1. [A].
Seule la première demi équation est correcte
2. Une
réaction d’oxydoréduction ne peut se faire qu’en milieu acide
3- En
milieu basique, l’équilibre des charges n’est pas respecté
4- L’aspect
milieu acide ou basique concerne aussi bien l’écriture des ½ équations que la
réaction d’oxydoréduction globale
L’affirmation
4 est exacte.
Affirmation
1
Non.
[A]. Les
deux ½ équations redox du permanganate de potassium sont correctes.
La
première, H+ côté réactifs : la réaction se fait en milieu
acide.
La
deuxième, ion hydroxyde côté produit : la réaction se fait en milieu
basique.
Affirmation
2
Non.
Réaction
redox en solution aqueuse avec des H+
côté réactifs : l’équation est favorisée en milieu acide (nécessité
de beaucoup de protons pour la réaction).
Réaction
redox en solution aqueuse avec des H+
côté produits (ou des HO-) : l’équation est favorisée en
milieu basique.
Affirmation
4
Oui.
L’aspect
milieu acide ou basique concerne aussi bien l’écriture des ½ équations que la
réaction d’oxydoréduction globale.
Voir pages suivantes
Page 5.
Electrolyse de l’eau
Sélectionner
l’affirmation exacte :
1. [A].
Caractère oxydant de l’eau
2. [B].
L’addition des 2 ½ équations en milieu basique ne donne pas le même résultat
que l’addition des 2 ½ réactions du milieu basique
3-
L’électrolyse de l’eau donne un ion hydroxyde et un ion H+
4-
L’électrolyse de l’eau donne 2 fois plus d’hydrogène que d’oxygène
L’affirmation
4 est exacte.
Affirmation
1
Non.
[A].
Caractère réducteur de l’eau
Dans
cette ½ équation l’eau perd des électrons pour s’oxyder en O2.
L’eau est
ici un réducteur.
Rappels :
Un
réducteur « rend », un réducteur s’oxyde.
Oxydation :
perte d’électrons par un réducteur.
(Une
réduction est un gain
2 H2O
perdent des électrons pour s’oxyder en O2 : la perte de 2 atomes d’hydrogène = perte des 2 électrons
(1 par atome).
Affirmation
3
Non.
Ne pas
confondre :
- Hydratation,
dissociation en solution aqueuse
H2O
s’hydrate, se dissocie, en ion hydroxyde HO- et proton H+.
Voir Autoprotolyse
de l’eau
- Hydrolyse d’une molécule : rupture d’une liaison moléculaire et création de nouvelles molécules sous l’effet de
l’eau ou d’un courant électrique.
L’eau
s’hydrolyse en H2 et O2.
Voir Hydratation/hydrolyse
Page 6.
Potentiels redox, pH,
chimique
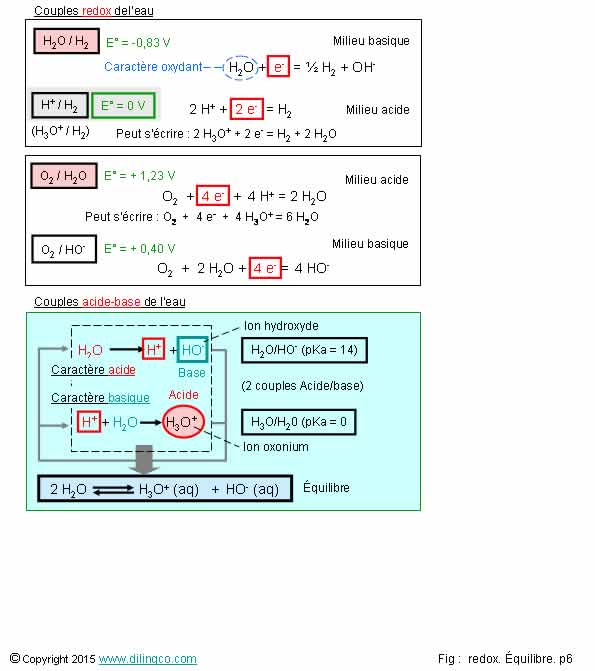
Sélectionner
l’affirmation exacte :
1- Les
potentiels standard de l’eau ont tous la même valeur
2- Les
ions pour définir les pH et les potentiels redox standard de l’eau sont
différents
3- Le potentiel
redox standard de l’eau en milieu acide a été choisi comme référence de
l’échelle des potentiels standard
4- Potentiel
chimique = Potentiel hydrogène = Potentiel redox = E°= 7
L’affirmation
3 est exacte.
Affirmation
2
Non.
Ions de
dissociation de l’eau : H+, HO-
Affirmation
4
Non.
Ne pas
confondre :
- potentiel
chimique, (lié à l’énergie libre, l’enthalpie libre G)
- potentiel
hydrogène (pH),
- potentiel
redox (force électromotrice).
Le
potentiel chimique m(T,P) d’un élément chimique est
l’énergie ajoutée lorsqu’on introduit une mole de cet élément.
Le potentiel redox de l’eau forme acide, fem de l’eau pure, se
mesure en volts. E° eau = 0V.
pH neutre de l’eau pure =7
pH = -
log (concentration des ions H3O+)
pH
neutre : (concentration ions H3O+) = (concentration
HO-) = 14/2 = 7
Page 7.
Oxydation & réduction
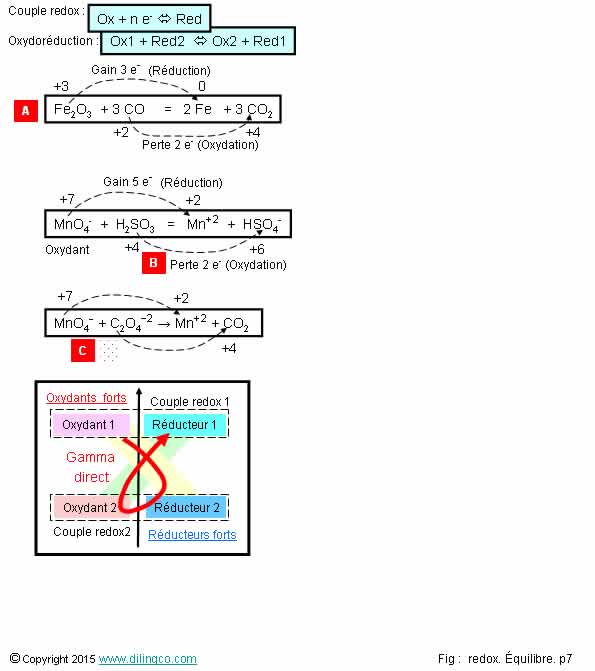
Sélectionner
les deux affirmations exactes :
1- Oxydoréduction :
au moins 1 élément gagne un électron et 1 élément perd un électron =
variation de n.o. de part et d’autre de l’équation
2-
Oxydoréduction : Ox couple1 + Red couple1 = Ox couple 2 + Red couple 2
3- [A].
CO : oxydant
4- [B].
+4 à +6 = gain de 2 électrons
5- [C].
+3
6- Les
équations présentées sont équilibrées
Les
affirmations 1 et 5 sont exactes.
Affirmation
2
Oxydoréduction :
Ox1 +
Red2 = Ox2 + Red1
La
réaction redox favorisée par la thermodynamique se fait dans le sens des
réactifs forts (Ox1 & Red2) pour donner des produits faibles (ox2 &
Red1).
Voir Règle du gamma redox
Affirmation
3
Non.
[A].
CO : réducteur.
CO perd 2
électrons pour donner du CO2.
Une perte d’électrons est une oxydation.
Un réducteur s’oxyde : CO est un réducteur.
Affirmation
4
Non.
[B]. +4 à
+6 = perte de 2 charges = perte de 2 électrons
Perte d’électrons = oxydation
Affirmation
5
Non.
n.o. C2O4
= -2
C2 (4x-2)
= -2
C = 6/2 =
+3
Passage
de +3 à +4 = oxydation
Affirmation
6
Non.
Les
équations présentées ne sont pas équilibrées, ni en charges, ni en conservation
matières.
Page 8.
Équilibrage redox bilan
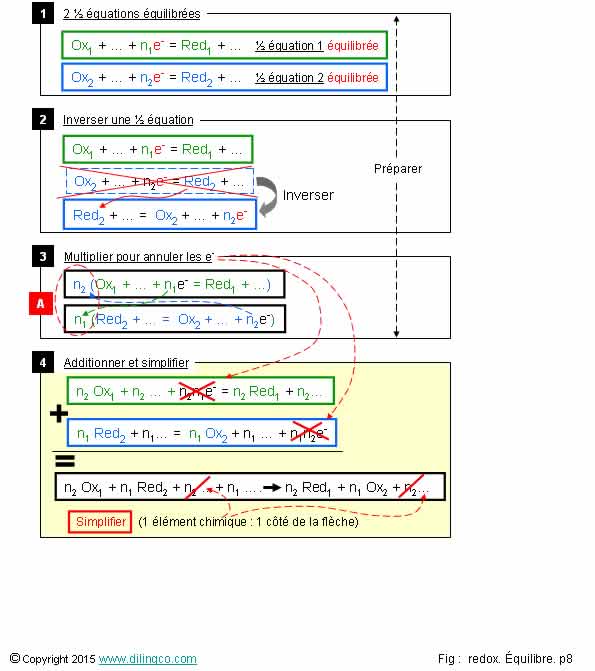
Sélectionner
l’affirmation exacte :
1- Étape
[1] : Les ½ équations sont identiques en milieu acide ou en milieu basique
2- [A].
Choisir les coefficients multiplicateurs pour qu’il n’y ait pas d’électrons
dans l’équation redox bilan
3- La
simplification de l’équation bilan consiste simplement à annuler les électrons
échangés
4- Après
simplification de l’équation bilan, il ne peut pas rester des H+ (ou des HO- en
milieu basique)
L’affirmation
2 est exacte.
Affirmation
1
Non.
Étape
[1] :
- milieu acide : Les ½ équations en sont
écrites avec des ions H+
- milieu basique : Les ½ équations en sont
écrites avec des ions HO-
Voir page précédente « Milieu acide. Milieu basique »
Affirmation
2
Oui.
[A].
Choisir les coefficients multiplicateurs les plus petits pour qu’il n’y ai pas
d’électrons dans l’équation redox bilan.
(Ou
simplement multiplier chaque équation par le coefficient d’électrons de l’autre)
Affirmation
3
Non.
Simplification
de l’équation bilan :
- annuler
les électrons échangés (les n1n2 e-),
- simplifier
chaque élément chimique pour le faire apparaître que d’un seul côté de la
flèche.
Le signe «=» des ½ équations doit être remplacé par une flèche de
sens de réaction redox.
Affirmation
4
Si.
Après
simplification, il peut rester des H+ (ou des HO- en milieu basique).
Exemple :
Avant simplification :
2
MnO4- +16H+ +10e- +5H2C2O4
-> 2Mn2+ + 8H2O + 10CO2 + 10H+
+ 10e-
Après simplification :
2
MnO4- + 6H+
+5H2C2O4 -> 2 Mn2+ + 8 H2O + 10CO2
Page 9.
Équilibrage redox.
Exercice

Sélectionner
l’affirmation exacte :
1- [A]. 2
e-
2- [B].
25 e-
3- [C]. 1
H+
4- [D]. 5
H2O
L’affirmation
3 est exacte.
Page 10.
Exemple de dosage
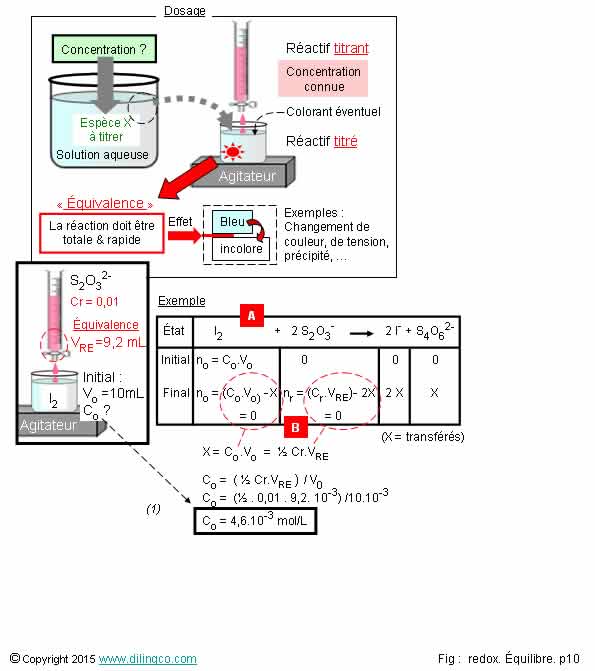
Sélectionner
l’affirmation exacte :
1-
Dosage : la connaissance du volume de réactif titrant pour arriver à
l’équivalence est suffisant pour déterminer la concentration du réactif à
titrer
2- À
l’équivalence, le nombre d’électrons que peut capter l’oxydant = nombre
d’électrons que peut céder le réducteur
3- À
l’équivalence, même si les réactifs sont dans les proportions
stoechiométriques, il reste du réactif titré
4- [A].
Le réactif I2 est le réducteur. [B]. À l’état final d’équivalence, nombre de
moles no=2, nr=1
L’affirmation
2 est exacte.
Affirmation
1
Non.
En plus
du volume de réactif titrant, il faut la concentration
molaire volumique Cr du
titrant.
Possédant
la concentration du réactif titrant, connaissant l’équation redox, la
concentration à titrer peut se calculer.
Voir figure (1).
Affirmation
3
Non.
À l’équivalence, les réactifs dans les proportions
stoechiométriques sont intégralement consommés.
Avant l’équivalence : manque de réactif titrant (Le réactif titrant est
limitant).
Après
l’équivalence, le réactif limitant est le réactif à titrer (il n’en reste plus
dans le bêcher).
Proportions
stoechiométriques, figure : il faut deux fois
plus de réactif tirant que de réactif à titrer pour arriver à
l’équivalence.
Affirmation
4
Non.
[A].
Le
réactif I2 est un oxydant :
il obtient des électrons.
Le réactif
S2O32- est un réducteur,
il rend des électrons.
Revoir Couple redox, nombres
d’oxydations
[B].
À l’état
final d’équivalence : les réactifs sont
entièrement consommés.
Nombre de
moles n oxydant = n réducteur = 0.
Exemple
de la figure
Solution
aqueuse de diiode I2, concentration inconnue, à titrer.
Titrant :
solution de thiosulfate S4O62- / S2O32-
Concentration
connue, volume à verser déterminé par l’ajout progressif de titrant dans la
solution à titrer et par le cchanement brusque de couleur à l’équivalence.
(Titrage colorimétrique)
½
équations:
S4O6-(aq)
+2 e- = 2 S2O3 2-(aq)
I2
(aq) + 2 e- = 2 I-(aq)
Les QCM interactifs sont accessibles à partir de la page d’accueil
du coaching virtuel à accès gratuit dilingco.com
Page 1.
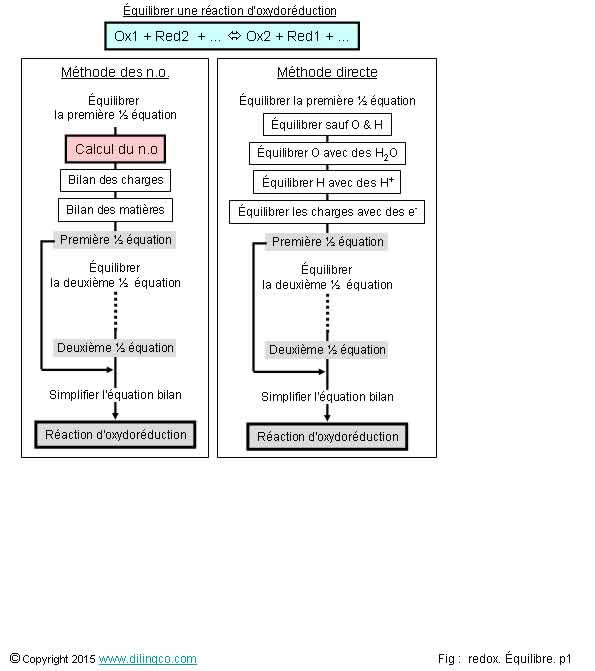
2 méthodes d’équilibrage redox

Sélectionner l’affirmation exacte :
1- Calculer le nombre d’oxydation est indispensable pour équilibrer une réaction d’oxydoréduction
2- Le nombre d’oxydation (n.o.) est la charge électrique réelle ou fictive d’un élément chimique
3- Le nombre d’oxydation d’un ion est nul
4- Le nombre d’oxydation d’une molécule est différent de 0
L’affirmation 2 est exacte.
Affirmation 1
Non.
2 méthodes sont à disposition pour équilibrer une réaction d’oxydoréduction.
Les 2 méthodes donnent le même résultat.
Utiliser le n.o. pour équilibrer une réaction d’oxydoréduction n’est donc pas indispensable.
Mais, dans une équation chimique, une variation du nombre d’oxydation indique à coup sûr qu’il s’agit d’une réaction d’oxydation.
Le n.o.
permet aussi de déterminer l’élément qui s’oxyde.
(Élément qui s’oxyde = réducteur)
Affirmation 2
Oui.
Le nombre d’oxydation (n.o.) :
- aussi appelé « degré d’oxydation », d.o.
- se note conventionnellement en chiffres romains,
- est la charge électrique réelle ou fictive d’un élément chimique,
- peut apparaître dans les annotations:
Oxyde de fer (II) : FeO, le fer a un n.o. = II
Oxyde de fer (III) : Fe2O3, le fer a un n.o. = III
Ces exemples montrent qu’un même atome peut avoir plusieurs valeurs de n.o. selon la molécule où il se trouve.
Affirmation 3
Non.
Le nombre d’oxydation d’un ion est égal à sa charge électrique.
Exemples :
Cr3+, n.o. = III
CIO4-, n.o. = I
Affirmation 4
Non.
Une molécule n’a pas de charge électrique : Le nombre d’oxydation d’une molécule est nul.
Équilibrer une demi-équation redox c’est :
- Equilibrer le nombre d’éléments chimiques,
- Equilibrer le nombre de charges électriques,
- Si l’oxydant contient des atomes d’oxygène :
- Placer des ions H+ coté oxydant,
- Placer des molécules d’eau coté réducteur.
2 méthodes
Deux méthodes d’équilibrage :
- Méthode des nombres d’oxydation
(À utiliser pour les couples redox d’éléments chimiques simples)
- Méthode d’équilibrage direct par les 2 demi équations
Dans les deux procédures, commencer par équilibrer les éléments chimiques.
Placement des électrons
Les deux procédures divergent sur le moment où placer les électrons pour équilibrer les charges électriques.
n.o : placer les électrons au début, en fonction des nombres d’oxydation,
½ équations : placer les électrons en fin de procédure lorsque tous les composants sont placés et équilibrés.
Page 2.
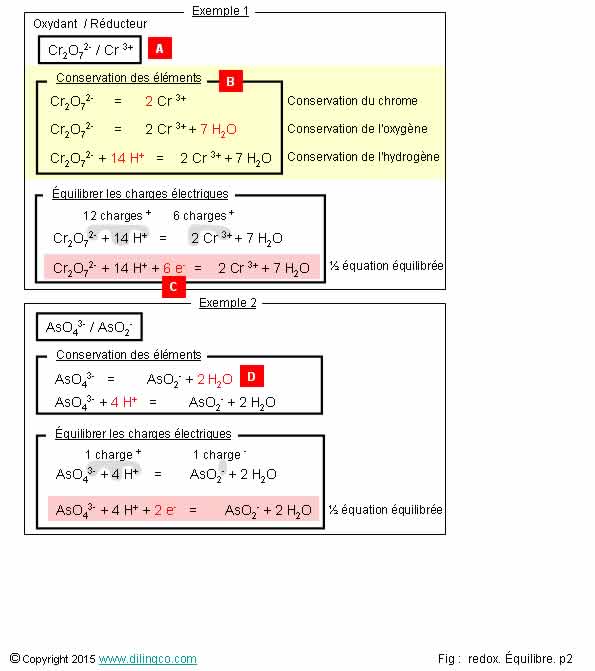
Méthode équilibrage matières

Sélectionner l’affirmation exacte :
1. [A]. Dans un couple redox, l’oxydant est le composé chimique qui a le moins de charges
2. [B]. Conservation des éléments chimiques : commencer toujours par équilibrer les éléments autres que O et H
3. [C]. Rajouter 5 électrons pour équilibrer les charges électriques
4. [D]. Rajouter O2 pour équilibrer les oxygènes
L’affirmation 2 est exacte.
Affirmation 1
Non.
[A]. L’oxydant :
- est celui qui est écrit à gauche du « / » (c’est une convention)
- est celui qui dans la demi équation « obtient » les électrons pour se réduire en réducteur
Rappels :
- un oxydant …se réduit,
- se réduit par une réaction de réduction pour former un réducteur.
Oxydation = perte d’électrons et formation d’un oxydant.
Réduction = gain d’électrons et formation d’un réducteur.
Affirmation 3
Non.
[C]. Rajouter 6 électrons pour équilibrer les charges électriques.
Côté gauche : 2 charges- + 14 charges+ = 12 charges+
Côté droit : 6 charges+
Rajouter 6 e- côté droit pour équilibrer les charges.
Affirmation 4
Non.
[D]. Rajouter 2H2O pour équilibrer les oxygènes.
Pour équilibrer l’excédent d’hydrogène causé par le rajout d’H2O, il faut :
- rajouter de H en milieu acide,
- rajouter des HO en milieu basique.
Équilibrer une demi-équation redox c’est :
- Equilibrer le nombre d’éléments chimiques,
- Equilibrer le nombre de charges électriques,
- Si l’oxydant contient des atomes d’oxygène :
- Placer des ions H+ coté oxydant,
- Placer des molécules d’eau coté réducteur.
2 méthodes
Deux méthodes d’équilibrage :
- Méthode des nombres d’oxydation
(À utiliser pour les couples redox d’éléments chimiques simples)
- Méthode d’équilibrage direct par les 2 demi équations
Dans les deux procédures, commencer par équilibrer les éléments chimiques.
Placement des électrons
Les deux procédures divergent sur le moment où placer les électrons pour équilibrer les charges électriques.
n.o : placer les électrons au début, en fonction des nombres d’oxydation,
½ équations : placer les électrons en fin de procédure lorsque tous les composants sont placés et équilibrés.
Page 3.
½ réaction. Méthode des n.o.

Sélectionner l’affirmation exacte :
1- Les nombres d’oxydation sont à calculer pour tous les composants des éléments de la ½ équation
2- [A]. La différence de n.o. a été calculée pour 1 atome Cr, comme il y en a 2 côté réactifs, il faut rajouter 2x(n.o) électrons
3- [B]. Différence de charges = 2
4- [C]. La ½ réaction est équilibrée du point de vue des charges et des matières
L’affirmation 2 est exacte.
Affirmation 1
Non.
Les nombres d’oxydation sont à calculer pour l’élément, présent des côtés oxydant/réducteur, caractéristique du couple considéré ; ici Cr.
Il faut bien entendu se rappeler les valeurs fondamentales des n.o. d’une molécule, d’un ion, de l’atome d’oxygène et d’hydrogène.
Revoir chapitre Nombres d’oxydation
Affirmation 3
Non.
[B]. Différence de charges : 6+ - (-8) = 14 charges positives à rajouter côté réactifs.
14 H+ sont rajoutés.
Affirmation 4
Non.
[C]. La ½ réaction sera équilibrée du point de vue des matières si on rajoute 2 H2O côté produits.
Valeurs n.o. à connaître
n.o. molécule = 0
n.o. ion = charge de l’ion
Le n.o. de l’atome d’oxygène est égal à –II
Exceptions :
- les peroxydes (H2O2, Na2O2, K2O2, …), n.o. = -I.
- le dioxygène O2, n.o. = 0
Le n.o. de l’atome d’hydrogène est égal à +I.
n.o =+I car les atomes d’hydrogène, moins électronégatifs, cèdent leur e- aux atomes liés d’électronégativité plus élevée.
Exceptions :
- les hydrures, H combiné à un métal (NaH, LiH, KH, …), n.o. = -I
- le dihydrogène H2, n.o. = 0
Le n.o. du fluor est toujours égal à –I.
Page 4.
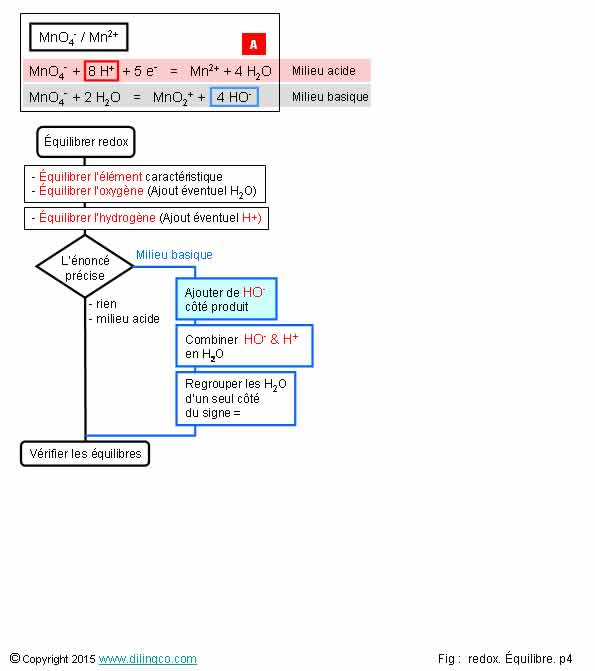
Milieu acide. Milieu basique

Sélectionner l’affirmation exacte :
1. [A]. Seule la première demi équation est correcte
2. Une réaction d’oxydoréduction ne peut se faire qu’en milieu acide
3- En milieu basique, l’équilibre des charges n’est pas respecté
4- L’aspect milieu acide ou basique concerne aussi bien l’écriture des ½ équations que la réaction d’oxydoréduction globale
L’affirmation 4 est exacte.
Affirmation 1
Non.
[A]. Les deux ½ équations redox du permanganate de potassium sont correctes.
La première, H+ côté réactifs : la réaction se fait en milieu acide.
La deuxième, ion hydroxyde côté produit : la réaction se fait en milieu basique.
Affirmation 2
Non.
Réaction redox en solution aqueuse avec des H+ côté réactifs : l’équation est favorisée en milieu acide (nécessité de beaucoup de protons pour la réaction).
Réaction redox en solution aqueuse avec des H+ côté produits (ou des HO-) : l’équation est favorisée en milieu basique.
Affirmation 4
Oui.
L’aspect milieu acide ou basique concerne aussi bien l’écriture des ½ équations que la réaction d’oxydoréduction globale.
Voir pages suivantes
Page 5.
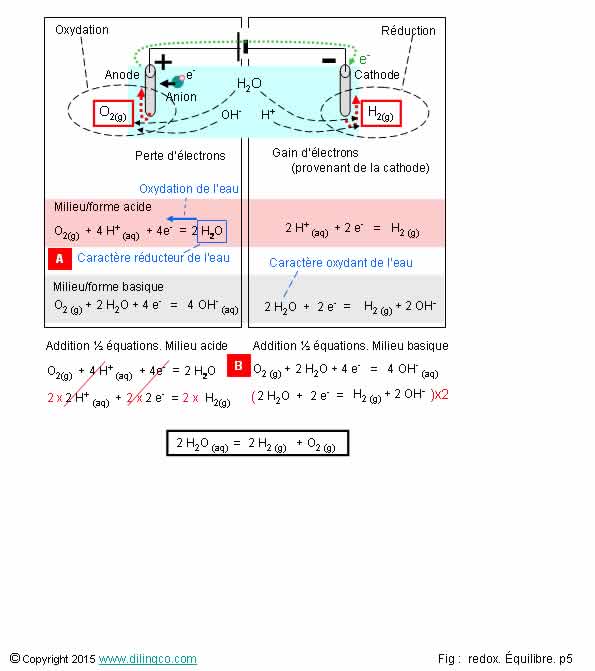
Electrolyse de l’eau

Sélectionner l’affirmation exacte :
1. [A]. Caractère oxydant de l’eau
2. [B]. L’addition des 2 ½ équations en milieu basique ne donne pas le même résultat que l’addition des 2 ½ réactions du milieu basique
3- L’électrolyse de l’eau donne un ion hydroxyde et un ion H+
4- L’électrolyse de l’eau donne 2 fois plus d’hydrogène que d’oxygène
L’affirmation 4 est exacte.
Affirmation 1
Non.
[A]. Caractère réducteur de l’eau
Dans cette ½ équation l’eau perd des électrons pour s’oxyder en O2.
L’eau est ici un réducteur.
Rappels :
Un réducteur « rend », un réducteur s’oxyde.
Oxydation : perte d’électrons par un réducteur.
(Une réduction est un gain
2 H2O perdent des électrons pour s’oxyder en O2 : la perte de 2 atomes d’hydrogène = perte des 2 électrons (1 par atome).
Affirmation 3
Non.
Ne pas confondre :
- Hydratation, dissociation en solution aqueuse
H2O s’hydrate, se dissocie, en ion hydroxyde HO- et proton H+.
Voir Autoprotolyse de l’eau
- Hydrolyse d’une molécule : rupture d’une liaison moléculaire et création de nouvelles molécules sous l’effet de l’eau ou d’un courant électrique.
L’eau s’hydrolyse en H2 et O2.
Voir Hydratation/hydrolyse
Page 6.
Potentiels redox, pH, chimique

Sélectionner l’affirmation exacte :
1- Les potentiels standard de l’eau ont tous la même valeur
2- Les ions pour définir les pH et les potentiels redox standard de l’eau sont différents
3- Le potentiel redox standard de l’eau en milieu acide a été choisi comme référence de l’échelle des potentiels standard
4- Potentiel chimique = Potentiel hydrogène = Potentiel redox = E°= 7
L’affirmation 3 est exacte.
Affirmation 2
Non.
Ions de dissociation de l’eau : H+, HO-
Affirmation 4
Non.
Ne pas confondre :
- potentiel chimique, (lié à l’énergie libre, l’enthalpie libre G)
- potentiel hydrogène (pH),
- potentiel redox (force électromotrice).
Le potentiel chimique m(T,P) d’un élément chimique est l’énergie ajoutée lorsqu’on introduit une mole de cet élément.
Le potentiel redox de l’eau forme acide, fem de l’eau pure, se mesure en volts. E° eau = 0V.
pH neutre de l’eau pure =7
pH = - log (concentration des ions H3O+)
pH neutre : (concentration ions H3O+) = (concentration HO-) = 14/2 = 7
Page 7.
Oxydation & réduction

Sélectionner les deux affirmations exactes :
1- Oxydoréduction : au moins 1 élément gagne un électron et 1 élément perd un électron = variation de n.o. de part et d’autre de l’équation
2- Oxydoréduction : Ox couple1 + Red couple1 = Ox couple 2 + Red couple 2
3- [A]. CO : oxydant
4- [B]. +4 à +6 = gain de 2 électrons
5- [C]. +3
6- Les équations présentées sont équilibrées
Les affirmations 1 et 5 sont exactes.
Affirmation 2
Oxydoréduction :
Ox1 + Red2 = Ox2 + Red1
La
réaction redox favorisée par la thermodynamique se fait dans le sens des
réactifs forts (Ox1 & Red2) pour donner des produits faibles (ox2 &
Red1).
Voir Règle du gamma redox
Affirmation 3
Non.
[A]. CO : réducteur.
CO perd 2 électrons pour donner du CO2.
Une perte d’électrons est une oxydation.
Un réducteur s’oxyde : CO est un réducteur.
Affirmation 4
Non.
[B]. +4 à
+6 = perte de 2 charges = perte de 2 électrons
Perte d’électrons = oxydation
Affirmation 5
Non.
n.o. C2O4 = -2
C2 (4x-2) = -2
C = 6/2 = +3
Passage de +3 à +4 = oxydation
Affirmation 6
Non.
Les équations présentées ne sont pas équilibrées, ni en charges, ni en conservation matières.
Page 8.
Équilibrage redox bilan

Sélectionner l’affirmation exacte :
1- Étape [1] : Les ½ équations sont identiques en milieu acide ou en milieu basique
2- [A]. Choisir les coefficients multiplicateurs pour qu’il n’y ait pas d’électrons dans l’équation redox bilan
3- La simplification de l’équation bilan consiste simplement à annuler les électrons échangés
4- Après simplification de l’équation bilan, il ne peut pas rester des H+ (ou des HO- en milieu basique)
L’affirmation 2 est exacte.
Affirmation 1
Non.
Étape [1] :
- milieu acide : Les ½ équations en sont écrites avec des ions H+
- milieu basique : Les ½ équations en sont écrites avec des ions HO-
Voir page précédente « Milieu acide. Milieu basique »
Affirmation 2
Oui.
[A]. Choisir les coefficients multiplicateurs les plus petits pour qu’il n’y ai pas d’électrons dans l’équation redox bilan.
(Ou simplement multiplier chaque équation par le coefficient d’électrons de l’autre)
Affirmation 3
Non.
Simplification de l’équation bilan :
- annuler les électrons échangés (les n1n2 e-),
- simplifier chaque élément chimique pour le faire apparaître que d’un seul côté de la flèche.
Le signe «=» des ½ équations doit être remplacé par une flèche de sens de réaction redox.
Affirmation 4
Si.
Après simplification, il peut rester des H+ (ou des HO- en milieu basique).
Exemple :
Avant simplification :
2 MnO4- +16H+ +10e- +5H2C2O4 -> 2Mn2+ + 8H2O + 10CO2 + 10H+ + 10e-
Après simplification :
2 MnO4- + 6H+ +5H2C2O4 -> 2 Mn2+ + 8 H2O + 10CO2
Page 9.
Équilibrage redox. Exercice

Sélectionner l’affirmation exacte :
1- [A]. 2 e-
2- [B]. 25 e-
3- [C]. 1 H+
4- [D]. 5 H2O
L’affirmation 3 est exacte.
Page 10.
Exemple de dosage

Sélectionner l’affirmation exacte :
1- Dosage : la connaissance du volume de réactif titrant pour arriver à l’équivalence est suffisant pour déterminer la concentration du réactif à titrer
2- À l’équivalence, le nombre d’électrons que peut capter l’oxydant = nombre d’électrons que peut céder le réducteur
3- À l’équivalence, même si les réactifs sont dans les proportions stoechiométriques, il reste du réactif titré
4- [A]. Le réactif I2 est le réducteur. [B]. À l’état final d’équivalence, nombre de moles no=2, nr=1
L’affirmation 2 est exacte.
Affirmation 1
Non.
En plus du volume de réactif titrant, il faut la concentration molaire volumique Cr du titrant.
Possédant
la concentration du réactif titrant, connaissant l’équation redox, la
concentration à titrer peut se calculer.
Voir figure (1).
Affirmation 3
Non.
À l’équivalence, les réactifs dans les proportions
stoechiométriques sont intégralement consommés.
Avant l’équivalence : manque de réactif titrant (Le réactif titrant est
limitant).
Après l’équivalence, le réactif limitant est le réactif à titrer (il n’en reste plus dans le bêcher).
Proportions stoechiométriques, figure : il faut deux fois plus de réactif tirant que de réactif à titrer pour arriver à l’équivalence.
Affirmation 4
Non.
[A].
Le réactif I2 est un oxydant : il obtient des électrons.
Le réactif S2O32- est un réducteur, il rend des électrons.
Revoir Couple redox, nombres d’oxydations
[B].
À l’état final d’équivalence : les réactifs sont entièrement consommés.
Nombre de moles n oxydant = n réducteur = 0.
Exemple de la figure
Solution aqueuse de diiode I2, concentration inconnue, à titrer.
Titrant : solution de thiosulfate S4O62- / S2O32-
Concentration connue, volume à verser déterminé par l’ajout progressif de titrant dans la solution à titrer et par le cchanement brusque de couleur à l’équivalence. (Titrage colorimétrique)
½ équations:
S4O6-(aq) +2 e- = 2 S2O3 2-(aq)
I2 (aq) + 2 e- = 2 I-(aq)